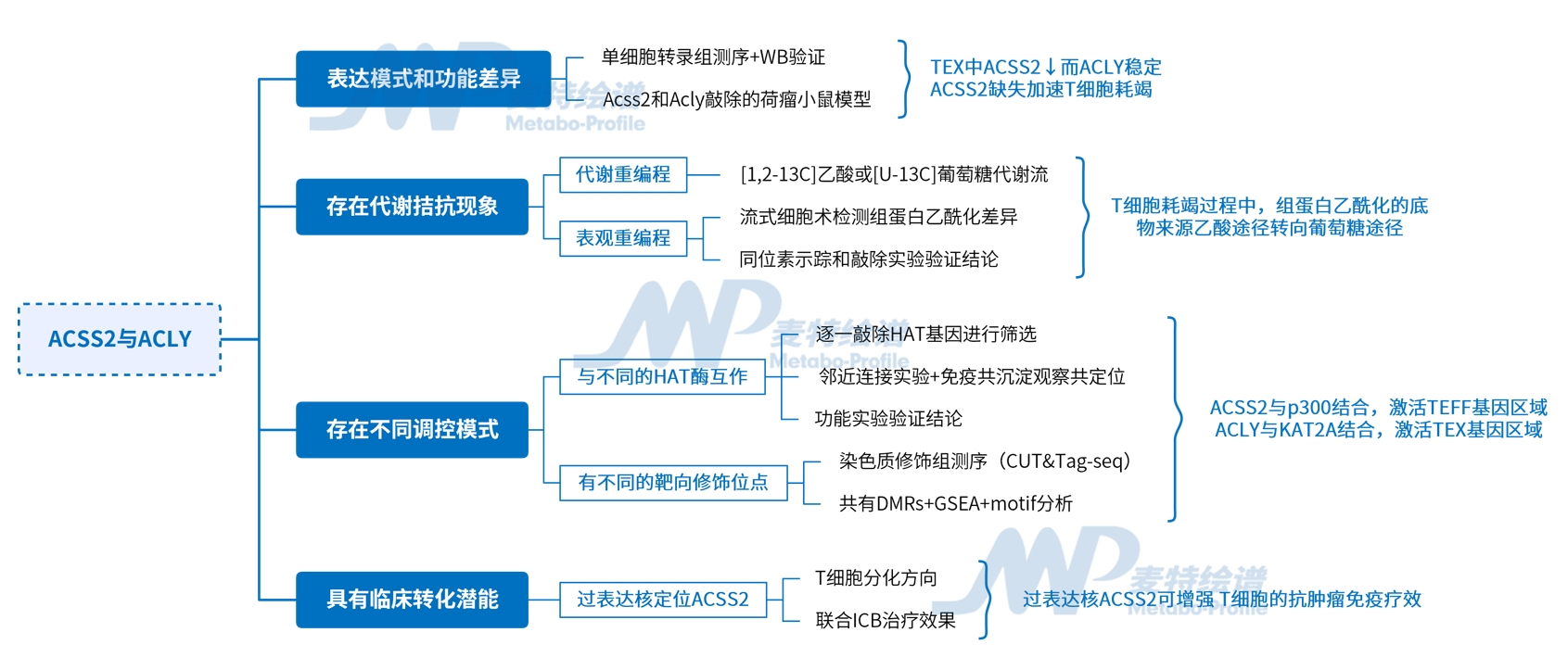
在癌症进展和免疫干预过程中,肿瘤特异性T细胞持续暴露于抗原刺激,逐步陷入功能耗竭状态(TEX)。这一过程并非骤然发生,而是经历精确的阶段性分化:最初是具有自我更新潜能的祖细胞状态(TEXprog),随后退化为功能受限的效应样状态(TEXeff),最终沦为彻底失能的终末耗竭状态(TEXterm)。在这三种细胞亚群中,TEXprog是免疫治疗的最后希望,此阶段T细胞对免疫检查点阻断治疗(ICB)仍具敏感性,而进入TEXterm后则难以逆转。
已有机制研究表明,T细胞耗竭的本质是代谢重编程与表观遗传调控失衡的协同作用。以组蛋白乙酰化修饰为例:在TEX细胞中,代谢重编程引起核内乙酰辅酶A区域性耗竭,导致H3K27ac等关键乙酰化标记在抗肿瘤基因(如IFN-γ、TNF-α)启动子区显著减少,形成转录沉默状态。这种耗竭表型通过DNA甲基化等机制稳定遗传,形成自我强化的恶性循环。
因此,研究者们思考:若能用某些方法矫正TEXprog的代谢-表观失衡,或许能阻止它发展成终末状态,这未尝不是一种免疫治疗的新思路。2024年12月,美国索尔克生物研究所的Susan M. Kaech团队在Science发表了题为“Nutrient-driven histone code determines exhausted CD8+T cell fates”的研究论文,聚焦TEX细胞代谢与表观遗传的互作机制,为优化肿瘤治疗策略提供了潜在干预靶点。
技术路线
研究结果
1. ACSS2与ACLY的表达模式和潜在功能均存在差异
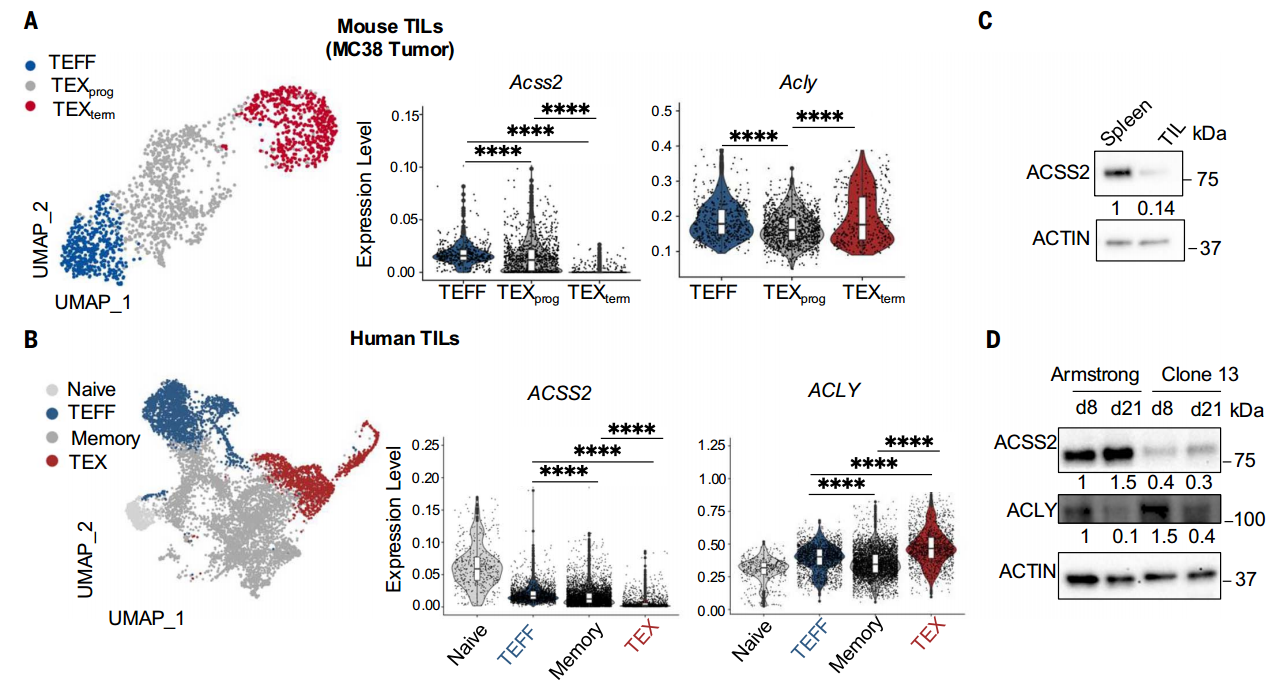
首先,研究者通过单细胞转录组测序分析发现,功能完整的效应CD8+T细胞(TEFF)高表达代谢酶ACSS2,而功能耗竭的T细胞(TEX)中ACSS2显著降低,其中TEXterm较TEXprog的ACSS2下调更为明显,且Western blot检测进一步验证了这一差异。值得注意的是,另一代谢酶ACLY在各T细胞亚群中表达稳定,提示其与ACSS2的调控机制存在本质区别。
在TEX细胞中,ACSS2表达量减少,而ACLY维持不变
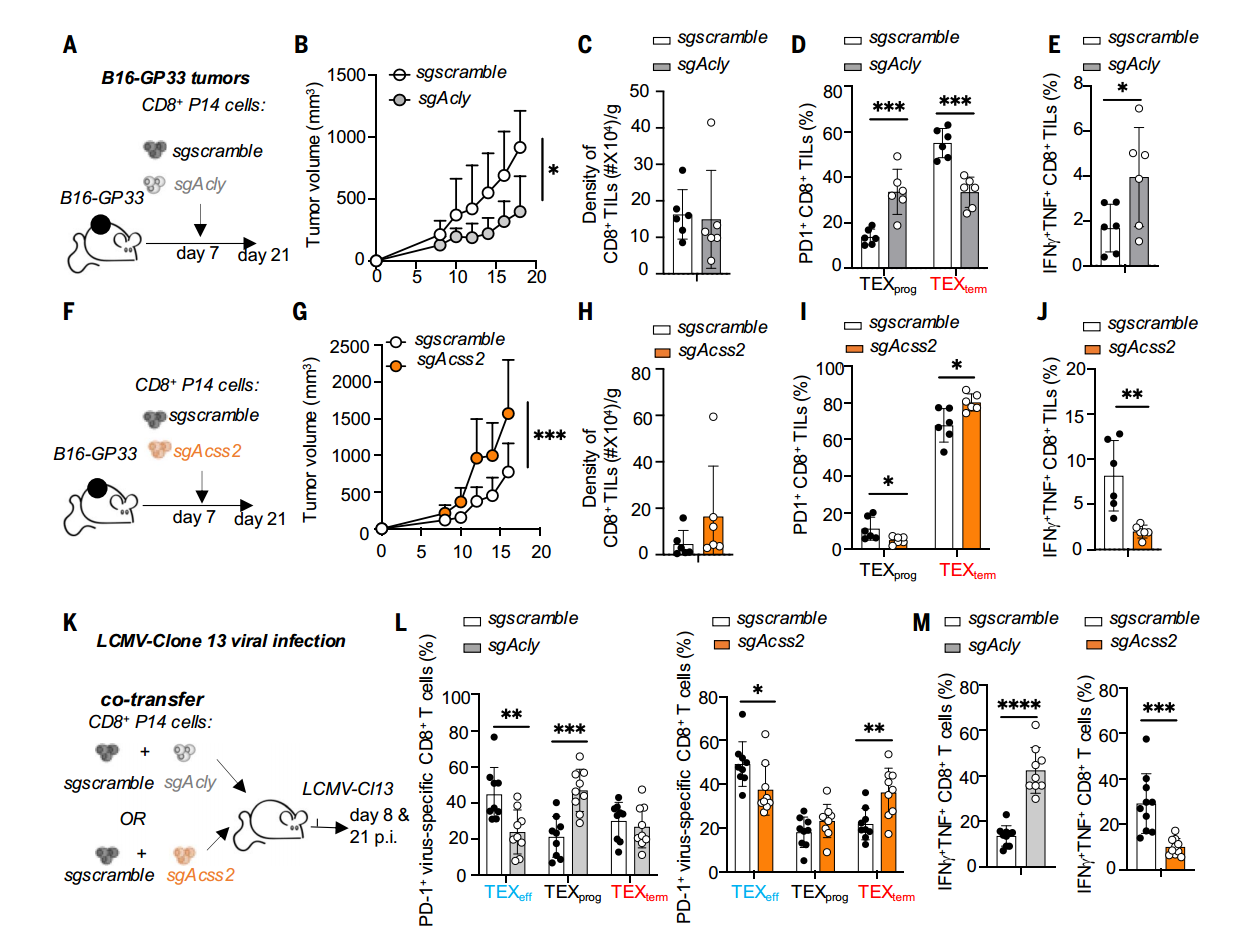
为明确二者的功能差异,研究者分别敲除TCR P14+CD8+T细胞的Acss2和Acly,然后过继转移至荷瘤及慢性感染小鼠模型,结果发现Acly缺陷型TILs表现出更强的肿瘤抑制能力,而Acss2缺失则导致T细胞完全丧失抗肿瘤活性。随后的机制研究表明,Acly敲除促使TCF-1+TEXprog亚群显著扩增,并伴随IFN-γ+TNF+双阳性效应细胞比例升高;而Acss2缺失组则加速向TEXterm分化,表现为效应分子表达下调及细胞因子分泌功能受损。
ACSS2促进TEXprog分化、抗肿瘤和抗病毒反应,而ACLY抑制
2. ACSS2与ACLY的代谢拮抗:乙酰辅酶A来源切换驱动表观遗传失衡
基于上述发现,研究者提出科学假设:功能正常的效应T细胞(TEFF)与耗竭T细胞(TEX)可能通过不同代谢途径(乙酸或葡萄糖)生成乙酰辅酶A。为此进行了稳定同位素示踪实验,分别从急/慢性感染小鼠中分离TEFF与TEX细胞,使用[1,2-13C]乙酸或[U-13C]葡萄糖进行4小时稳态标记,通过质谱检测代谢通量差异。结果显示,相较于TEFF细胞,TEX细胞内乙酸来源的M2标记乙酰辅酶A显著减少,而葡萄糖来源的标记比例升高,表明TEX细胞更依赖葡萄糖而非乙酸途径生成核内乙酰辅酶A,这与ACSS2表达下调的特征一致。
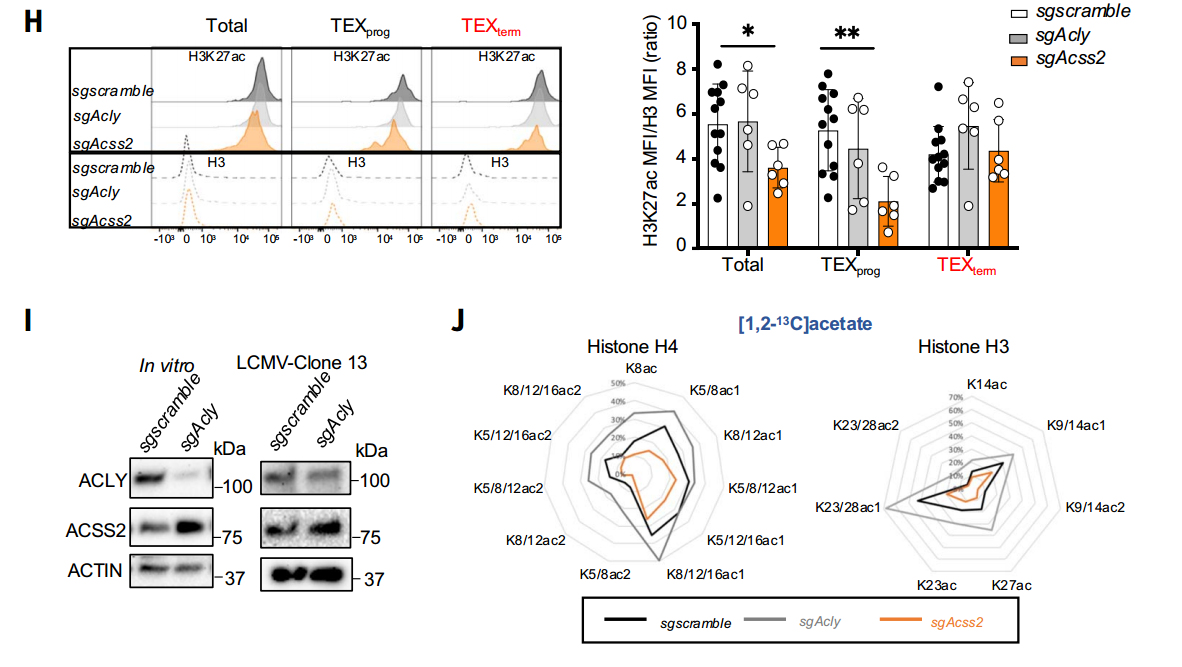
由于乙酰辅酶A是蛋白质乙酰化的直接底物,研究者进一步解析了TEX与TEFF细胞的组蛋白乙酰化差异。流式细胞术检测发现, TEX细胞的H3K27ac和H3K9ac水平较TEFF细胞显著降低,且TEXterm的修饰水平也低于TEXprog。同位素示踪实验进一步揭示,TEFF细胞优先利用乙酸来源的乙酰辅酶A进行组蛋白乙酰化,而TEX细胞转向依赖葡萄糖代谢供给。机制验证实验表明,敲除Acss2基因导致TEXprog细胞的H3K27ac水平下降50%,而Acly敲除对全局乙酰化无显著影响,甚至因ACSS2代偿性上调引发TEXterm细胞的H3K27ac水平回升。
ACSS2和ACLY差异调节TEFF和TEX细胞之间的乙酰辅酶A产生和组蛋白乙酰化
这些数据共同表明,CD8+T细胞从TEFF向TEX(尤其是TEXterm)分化过程中,组蛋白乙酰化的代谢来源从ACSS2介导的乙酸途径转向ACLY依赖的葡萄糖途径,但整体乙酰化水平仍呈进行性下降,提示代谢来源转换无法完全补偿表观遗传失衡。
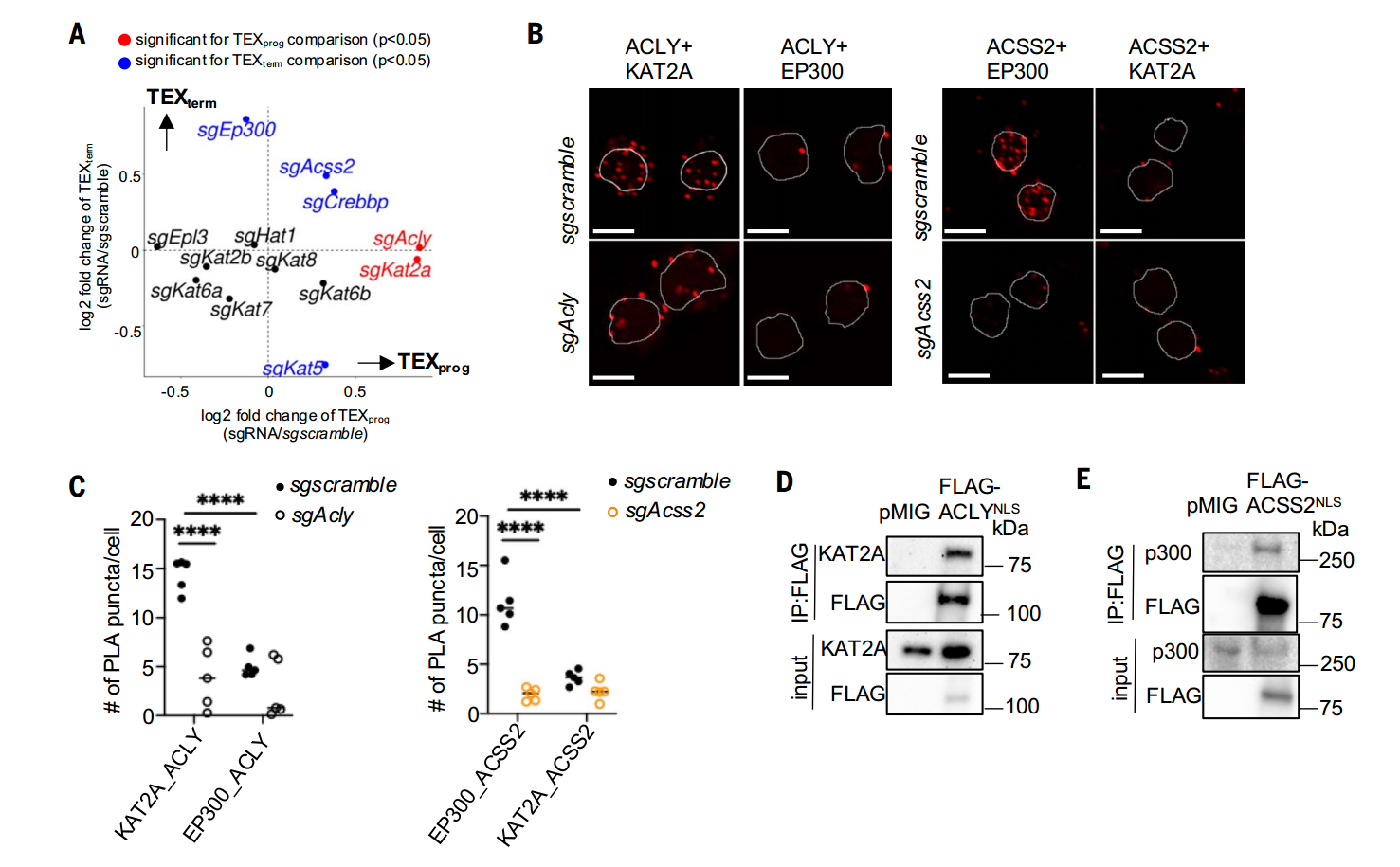
3. ACSS2与ACLY的调控机制:通过HAT特异性互作靶向不同的乙酰化位点
通过系统性敲除CD8+T细胞中的HAT基因,研究者发现:敲除p300或CBP促进TEXterm分化,而敲除KAT2A则增强TEXprog形成。邻近连接实验(PLA)结合免疫共沉淀进一步证实,ACLY与KAT2A在TEX细胞中形成特异性互作,而ACSS2与p300在TEFF细胞中共定位。功能验证实验表明,ACSS2依赖p300维持TEXprog相关位点的组蛋白乙酰化(如H3K27ac),而ACLY通过KAT2A驱动TEXterm特征基因的乙酰化修饰。这种代谢酶-HAT复合物的空间特异性互作揭示了T细胞分化命运的分子开关。
ACSS2和ACLY分别与p300和KAT2A相互作用
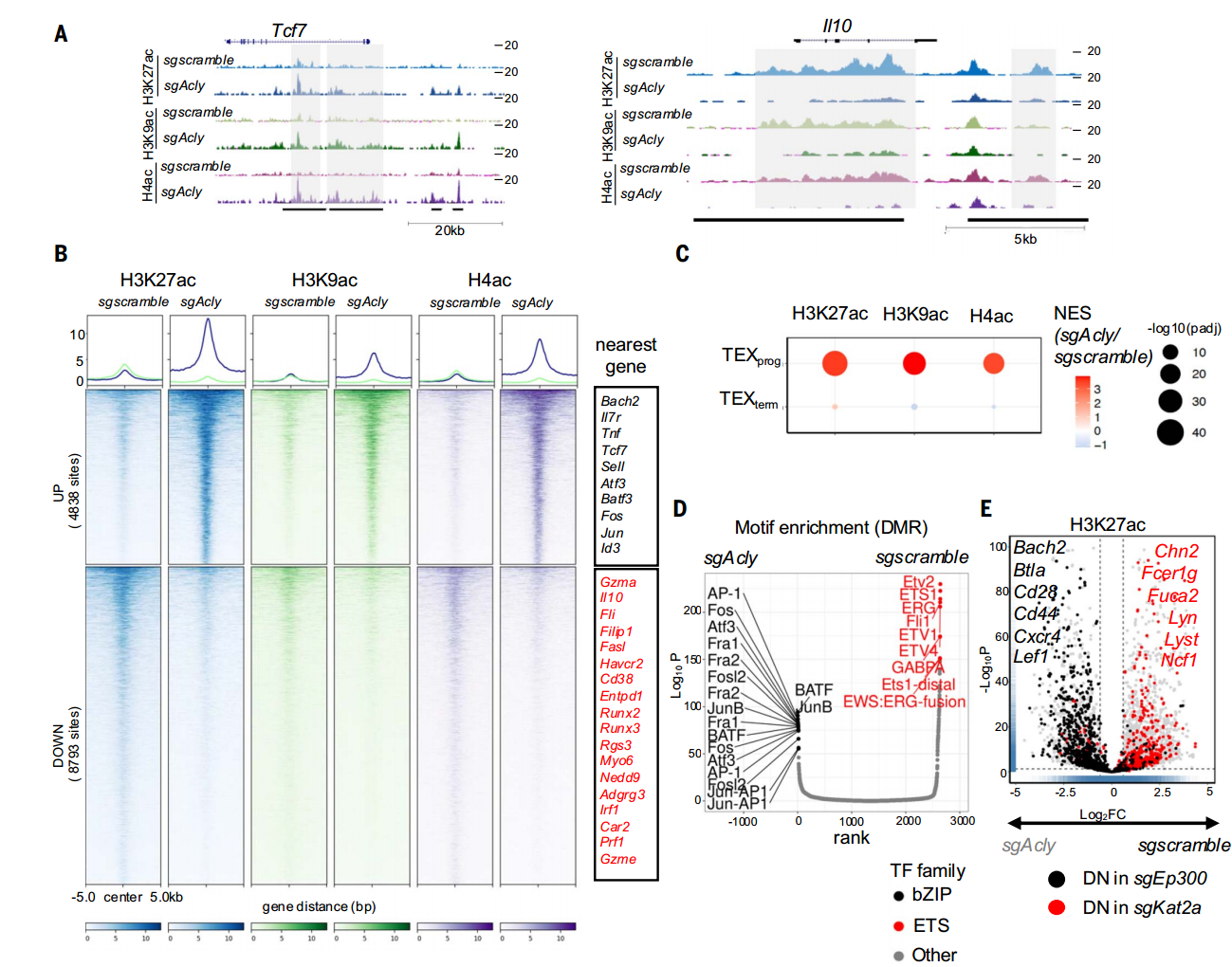
染色质修饰组分析(CUT&Tag-seq)表明代谢酶(ACSS2/ACLY)与HAT(p300/KAT2A)的复合物靶向不同染色质区域,从而调控T细胞向不同方向分化。
ACSS2和ACLY分别与p300和KAT2A协同调节基因座特异性组蛋白乙酰化
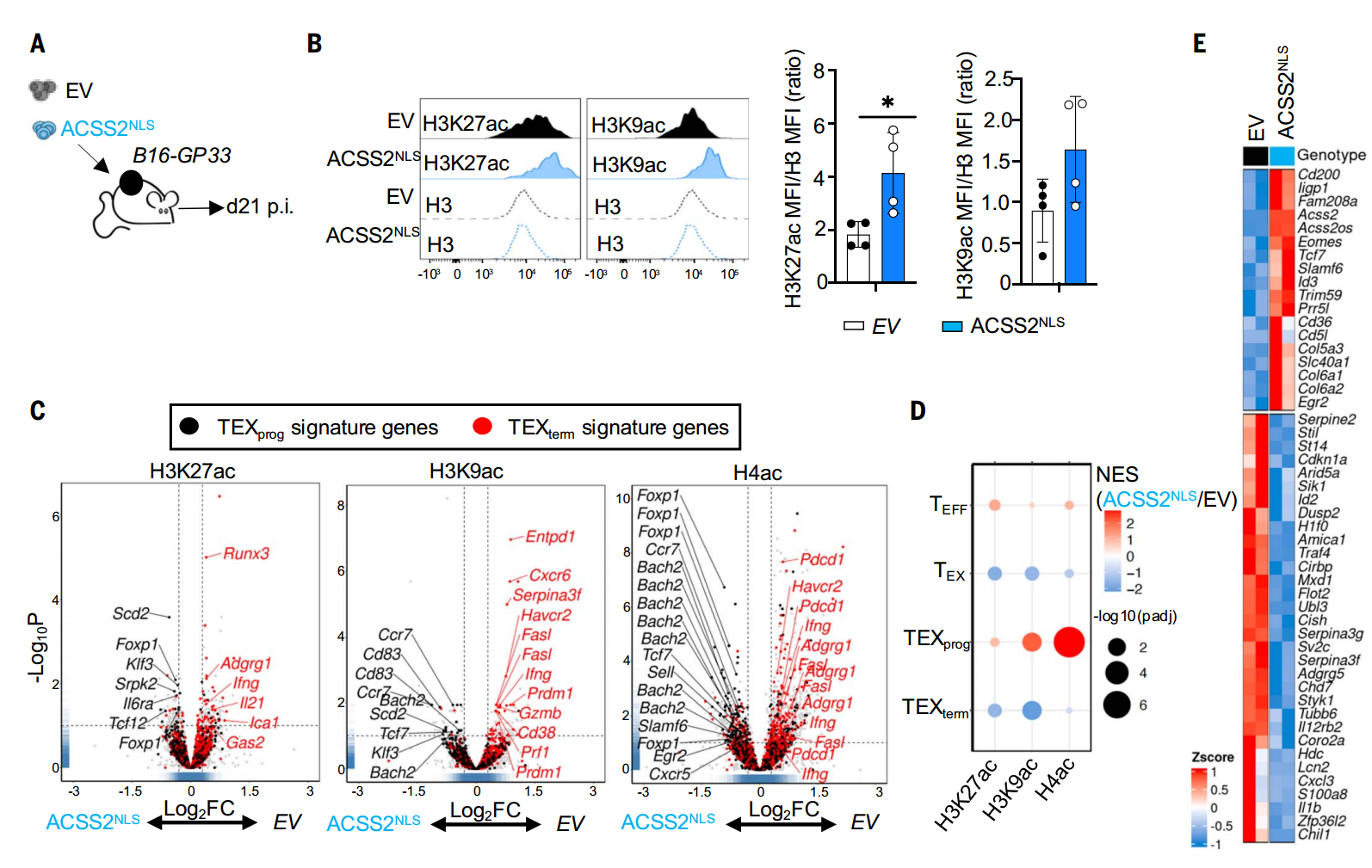
4. 临床转化潜能:核定位ACSS2增强T细胞干性,提升ICB疗效
最后,研究者通过荷瘤小鼠模型发现,核定位ACSS2过表达T细胞(ACSS2NLS-OE)可显著提升肿瘤浸润淋巴细胞(TILs)的组蛋白乙酰化水平,特异性富集TEXprog基因(Tcf7/Bach2)位点的乙酰化修饰。转录组显示ACSS2NLS-OE TILs中TEXprog基因上调而TEXterm基因受到抑制,证实核ACSS2通过表观重塑维持T细胞干性。此外,临床转化研究发现,ACSS2NLS的过表达联合ICB治疗可增强细胞因子分泌,控制肿瘤生长;值得注意的是,抑制葡萄糖代谢(ACLY抑制剂BMS-303141)也可代偿性上调ACSS2,协同ICB以CD8+T细胞依赖性方式显著抑制肿瘤进展。
过表达ACSS2促进TEXCL2相关位点的组蛋白乙酰化并增强基因表达
过表达核ACSS2或抑制ACLY均可增强CD8+T细胞的抗肿瘤免疫
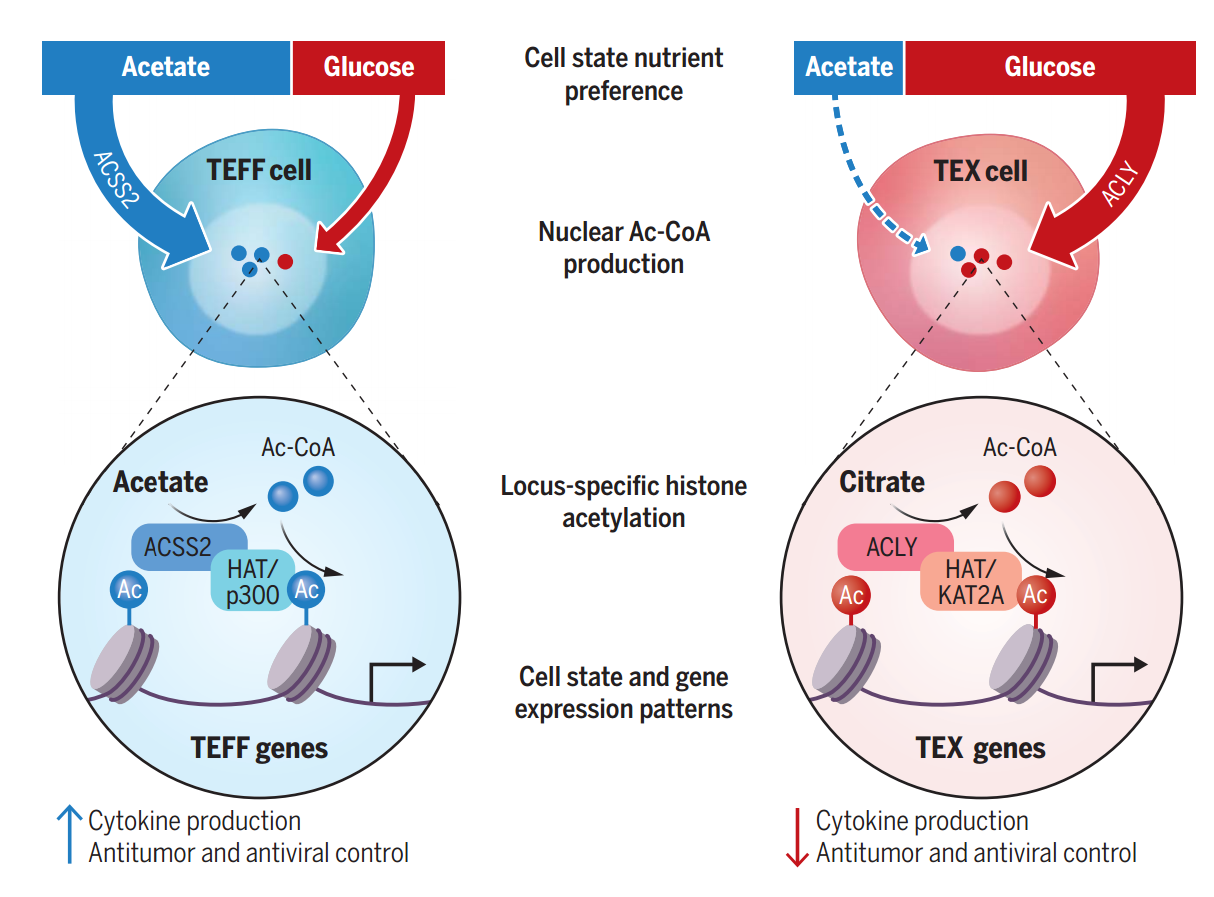
全文总结
本研究发现,代谢酶ACSS2与ACLY通过调控细胞核内乙酰辅酶A的生成,与组蛋白乙酰转移酶(HATs)协同作用,以染色质位点特异性的方式决定CD8+T细胞的分化方向。核定位的ACSS2突变体能显著增强干细胞样耗竭前体细胞(TEXprog)的生成;而抑制ACLY活性,可将终末耗竭的TEXterm细胞重编程为TEXprog状态。该研究不仅揭示了代谢与表观遗传互作在T细胞命运抉择中的核心地位,还为联合代谢干预(如ACLY抑制剂)与免疫检查点阻断提供了新思路,为优化过继性T细胞治疗策略奠定理论基础。
参考文献
Ma S, Dahabieh MS, Mann TH, et al. Nutrient-driven histone code determines exhausted CD8+T cell fates. Science. 2025
请扫描二维码阅读原文
绘谱帮您测
麦特绘谱提供全面的代谢流检测服务,可追踪含13C和15N等被标记物100+种,全面覆盖糖酵解和TCA循环通路、磷酸戊糖途径、 氨基酸代谢、脂肪酸代谢、 一碳代谢、 核苷酸代谢通路等。丰富的个性化标记定制经验–[U-13C6]-Fructose,[U-13C16]-Palmitate, [U-13C3]-Serine,[U-13C2]-Glycine, [U-13C3]-Alanine, [U-13C3]-Pyruvate, [U-13C4]Malic Acid, [U-13C18]-Oleic Acid, 13CO2, 15N-NH4CL, [1, 2-13C2]-Glucose, [2,3,3-D3]-Serine, [2,3-13C2]Alanine, [1,2,3-13C3]-Choline等。历经数年项目积累,检测各类贴壁细胞、悬浮细胞、菌体、培养液、线粒体、组织、粪便等样本类型,涵盖多发性骨髓瘤、肝癌、线粒体遗传代谢病、免疫细胞活性与疾病、心血管疾病等多个研究方向,合作项目成果突出,文章平均IF >10+。