中国医科大学附属盛京医院刘扬和孙思予教授研究团队通过研究表明脂滴形成在肝细胞癌(HCC)细胞对索拉非尼(sorafenib)的适应性中至关重要,并利用基于质谱的脂质组和蛋白质组揭示了其中重要的调控基因和作用机制。研究成果以“AKR1C3-dependent lipid droplet formation confers hepatocellular carcinoma cell adaptability to targeted therapy”为题,发表在Theranostics(IF:11.600)上。

研究结果
1.索拉非尼抗性的肝癌细胞中存在着脂肪酸氧化(FAO)向糖酵解转变导致的脂滴积累
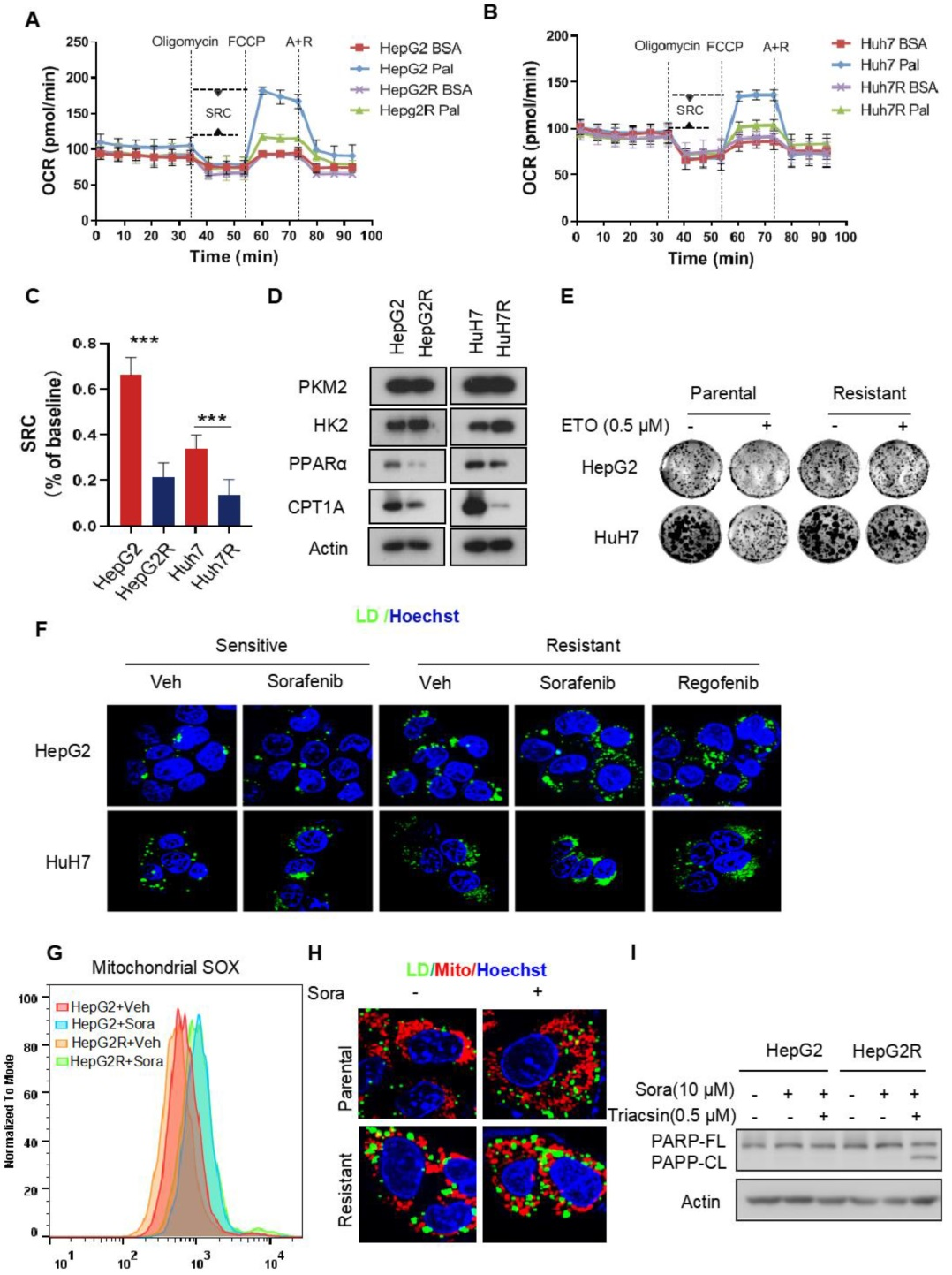
研究者首先构建了两株索拉非尼抗性的肝细胞癌(HCC)细胞系,分别为HepG2R 和HuH7R。随后,检测了索拉非尼抗性癌细胞的耗氧率(OCR)和细胞外酸化率(ECAR)。结果显示,抗性癌细胞的OCR下降,ECAR上升,ECAR/OCR的比率也显著上升。糖酵解代谢流检测发现,糖酵解增强。此外,研究还发现,抗性癌细胞完全废弃了脂肪酸氧化(FAO)。研究者进一步检测了细胞内无法被线粒体正常代谢的脂肪酸是否储存在脂滴中。结果显示,在索拉非尼和瑞戈非尼(Regorafenib)存在时,HepG2R 和HuH7R细胞里均检测到了清晰的脂滴。索拉非尼处理能增加原始癌细胞中线粒体活性氧(ROS)的产生,而在抗性癌细胞中仅有少量ROS的产生。此外,在抗性癌细胞的线粒体周围检测到了明显的脂滴积累,这表明脂肪酸(FA)转化为了甘油三酯(TAG)进行存储。为了确定脂滴形成是否对索拉非尼抗性有关键作用,研究者这使用Triacsin C对酰基辅酶A合成酶进行抑制进而阻止脂滴形成,结果抑制了索拉非尼抗性癌细胞的生长。
2. 脂质组学和蛋白质组学联合分析发现AKR1C3是TAG聚集的调控因子
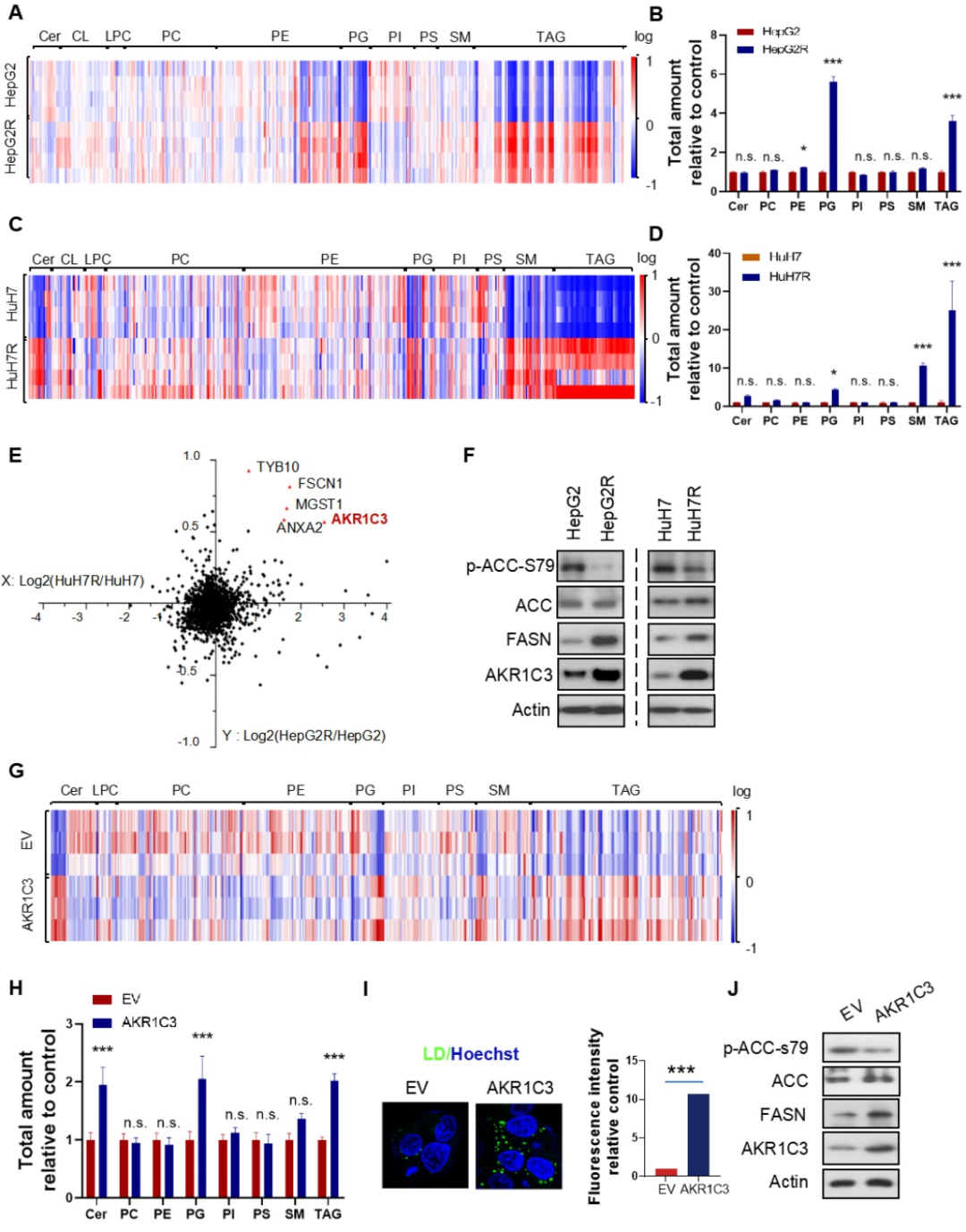
接下来,研究者对抗性癌细胞和原始癌细胞进行了脂质组学检测,结果显示TAG(甘油三酯)是在抗性癌细胞中上调最显著的代谢物,此外,前列腺素(PG)在抗性癌细胞中也普遍上调。为了找到调控TAG聚集的关键蛋白质,研究者对抗性癌细胞和原始癌细胞分别进行了蛋白质组学检测,有5个蛋白,包括HSD17B5 (AKR1C3)、TYB10、MGST1、 FSCN1和ANXA2在抗性癌细胞中上调。已有报道表明,AKR1C3与多囊卵巢综合征(PCOS)脂肪细胞中的脂质代谢和脂质形成相关,因此,研究者决定探究AKR1C3在肝细胞癌脂质代谢中的作用。
WB证实了AKR1C3在抗性癌细胞中的高表达。在抗性癌细胞中还检测到了脂肪酸合成酶(FASN)表达和乙酰辅酶A羧化酶(ACC)活性的上升。研究者构建了AKR1C3过表达的原始癌细胞HepG2-AKR1C3,并进行了脂质组学检测,结果显示HepG2-AKR1C3的脂质组学特征与抗性癌细胞的脂质组学特性相似,都有上升的甘油三酯(TAG)和前列腺素(PG)。此外,AKR1C3过表达通过下调p-ACC-s79和上调FASN的表达促进了脂质生成和脂滴产生,这与抗性癌细胞HepG2R中观察到的现象一致。综合以上结果表明,AKR1C3对脂滴形成有关键作用。
3. AKR1C3的缺失废除TAG(甘油三酯)的积累并刺激FAO(脂肪酸氧化)
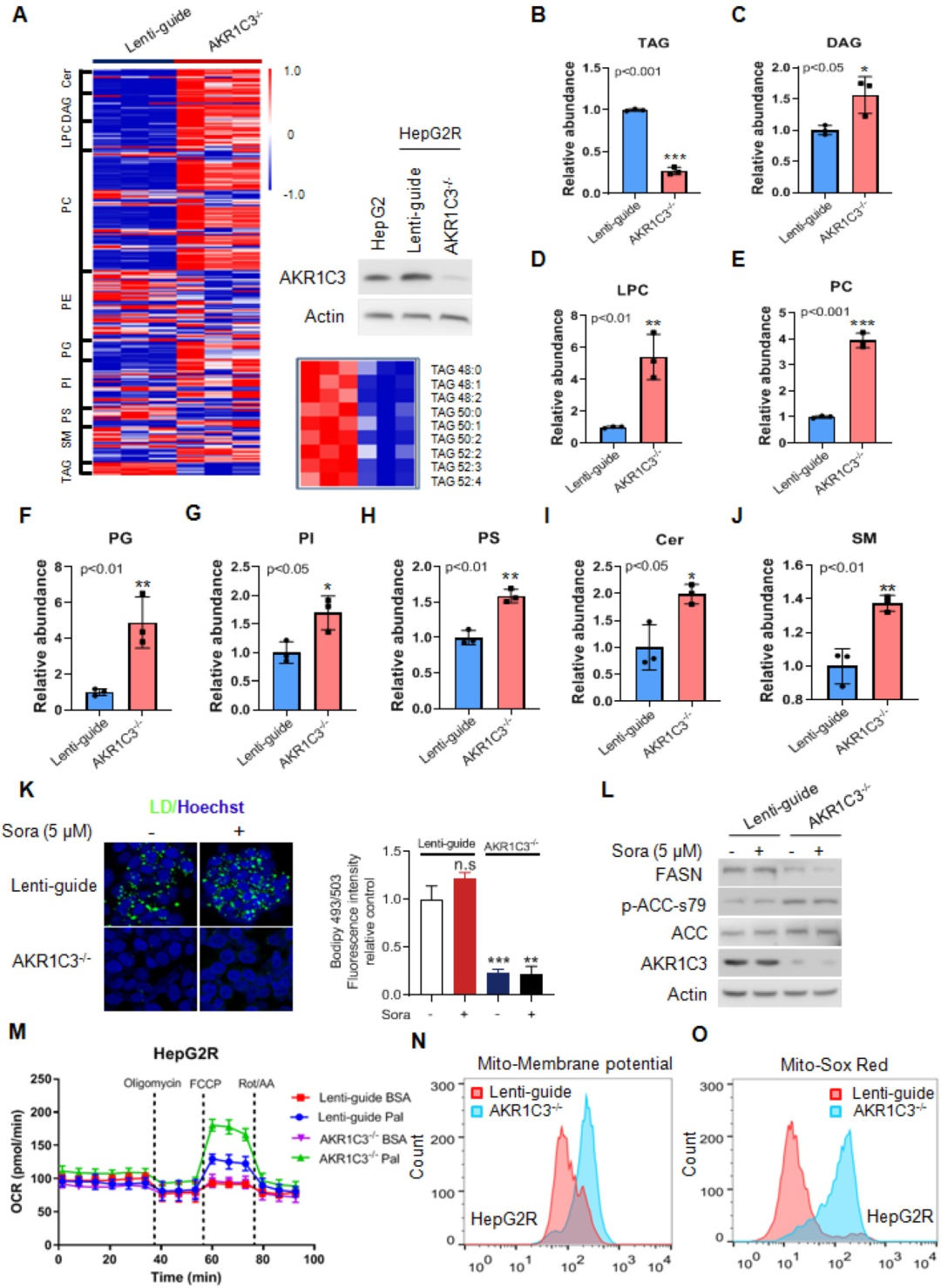
为了确定AKR1C3缺失是否影响肝细胞癌的脂质积累,研究者利用CRISPR/Cas9系统敲除了抗性癌细胞HepG2R中的AKR1C3并进行脂质组学检测。结果表明,最明显改变的代谢物富集在甘油磷脂代谢、甘油脂代谢和糖基磷脂酰肌醇(GPI)-锚定蛋白生物合成途径。此外,AKR1C3的缺失明显导致甘油三酯(TAG)的耗竭,以及二酰基甘油(DAG)、甘油磷脂(PC、LPC、PI、PS)和鞘磷脂(Cer、SM)种类的上调。此外,与对照组相比,AKR1C3-/-HepG2R细胞中的线粒体β-氧化增强。在AKR1C3-/-细胞中也明显观察到线粒体膜电位和活性氧(ROS)生成的增加。总之,这些结果证明,AKR1C3的缺失抑制了细胞内甘油三酯(TAG)的积累,促进了脂肪酸运输到线粒体进行β-氧化。
4. AKR1C3依赖的脂滴形成阻止线粒体功能障碍和脂肪毒性
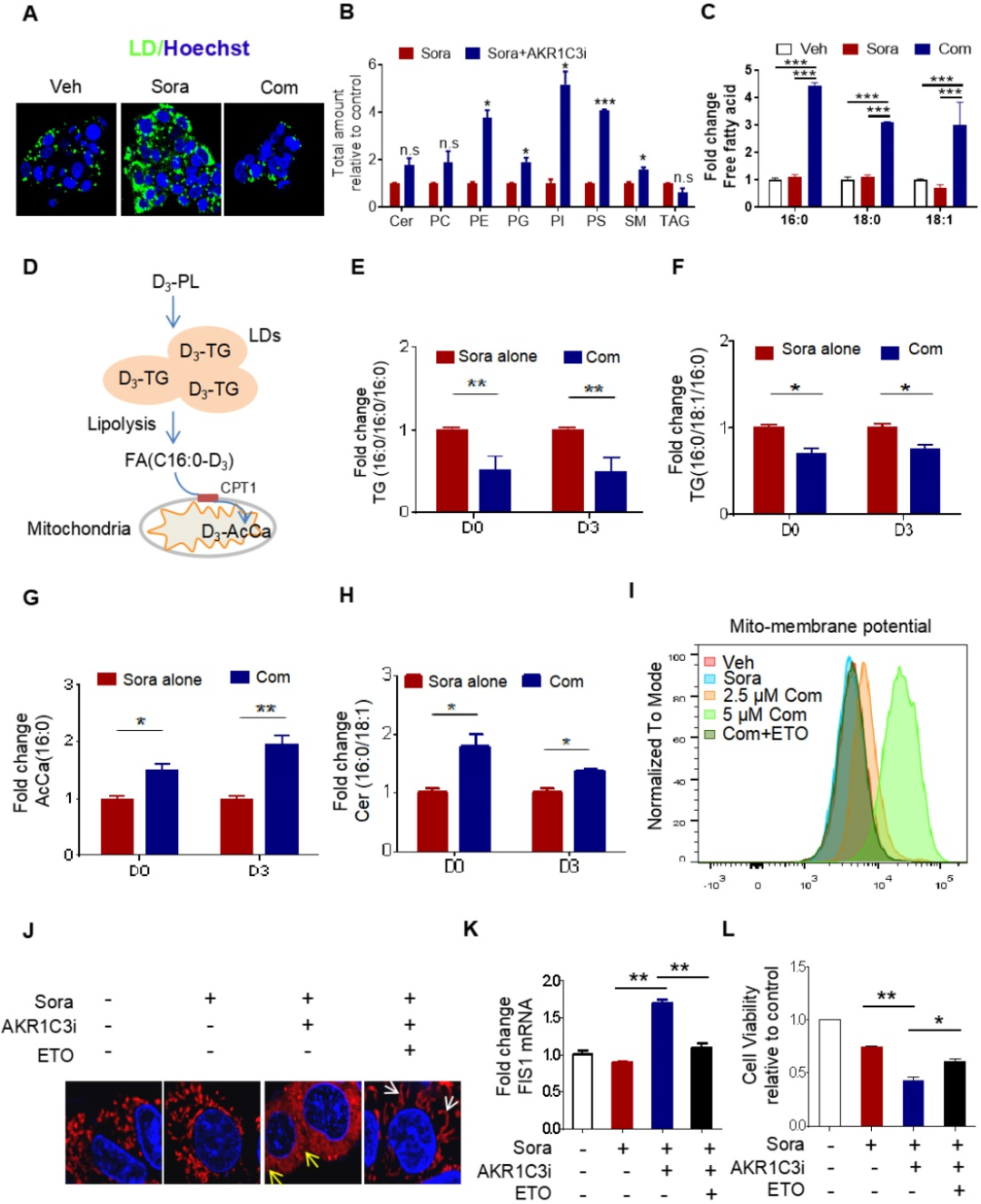
研究者假设AKR1C3通过抑制脂滴分解促进脂滴形成。因为在AKR1C3-/-细胞中存在脂滴积累,于是研究者使用两种AKR1C3的抑制剂,检测当AKR1C3活性被抑制后,是否会引起脂滴分解。研究者对AKR1C3抑制剂FLU(氟芬那酸)或5-βCA(5β-胆烷酸)处理后的抗性癌细胞HepG2R分别进行脂质组学检测。结果与AKR1C3-/-细胞相一致,在索拉非尼存在的条件下,抑制AKR1C3显著降低细胞甘油三酯(TAG)和脂滴的含量,而磷脂和鞘脂类脂质包括PE、PG、PI、PS和SM的含量则上升。同时还检测到抑制AKR1C3能显著降低甘油三酯(TAG)的减少以及细胞内游离脂肪酸(FFA)的增加,提示线粒体中β-氧化作用的减弱。研究者对线粒体功能的检测也发现抑制AKR1C3造成线粒体功能障碍。
5. AKR1C3抑制脂质自噬以支持脂滴形成
接下来研究者探究AKR1C3是如何调控脂质积累的。鉴于AKR1C3的基本功能是调控PG(前列腺素)合成,研究者首先检测了PG代谢是如何促进脂质积累的。结果表明AKR1C3介导的索拉非尼抗性和脂滴积累是PG非依赖性的。
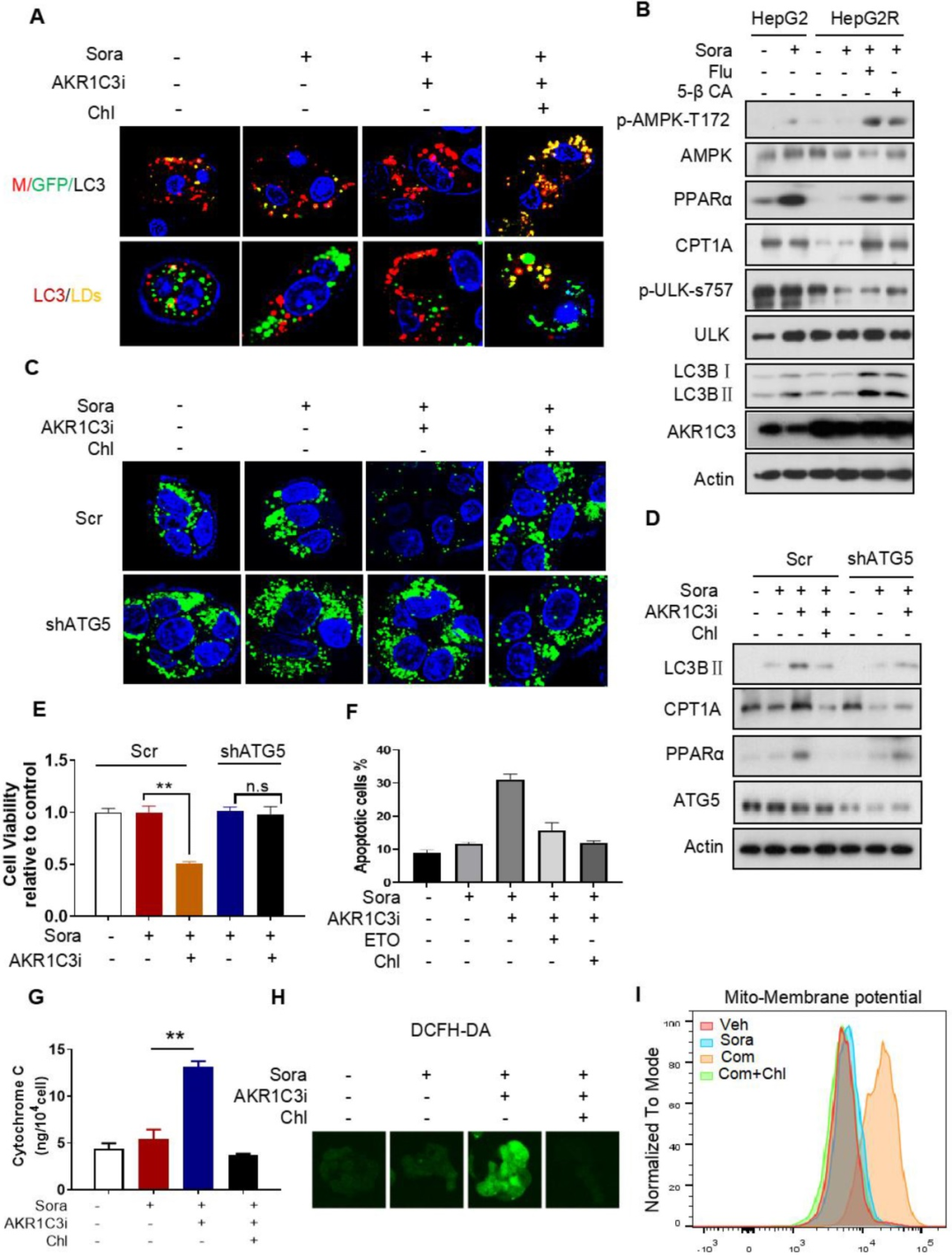
已有研究表明,抑制AKR1C3能增强胃肠癌细胞系中阿霉素诱导的细胞自噬,因此研究者假设AKR1C3可能通过自噬介导的脂滴分解(脂质自噬)调控脂滴稳态。通过mCherry-GFP-LC3 融合蛋白实验表明,抑制AKR1C3能增强细胞自噬。加强细胞自噬能在AKR1C3抑制的条件下诱导更显著的脂滴清除,而这种清除作用会被自噬抑制剂减弱。进一步研究发现,在AKR1C3抑制剂和索拉非尼联合处理条件下,自噬/脂质自噬的抑制或者敲低ATG5都能显著增强细胞生存,减少凋亡细胞数量,细胞显示出减少的细胞色素C释放和活性氧(ROS)生成,并有脂滴的增加,且线粒体膜电位能恢复到正常区间。综合以上结果表明,AKR1C3通过脂质自噬调控脂滴稳态。
6. AKR1C3促进代谢从氧化磷酸化转向糖酵解
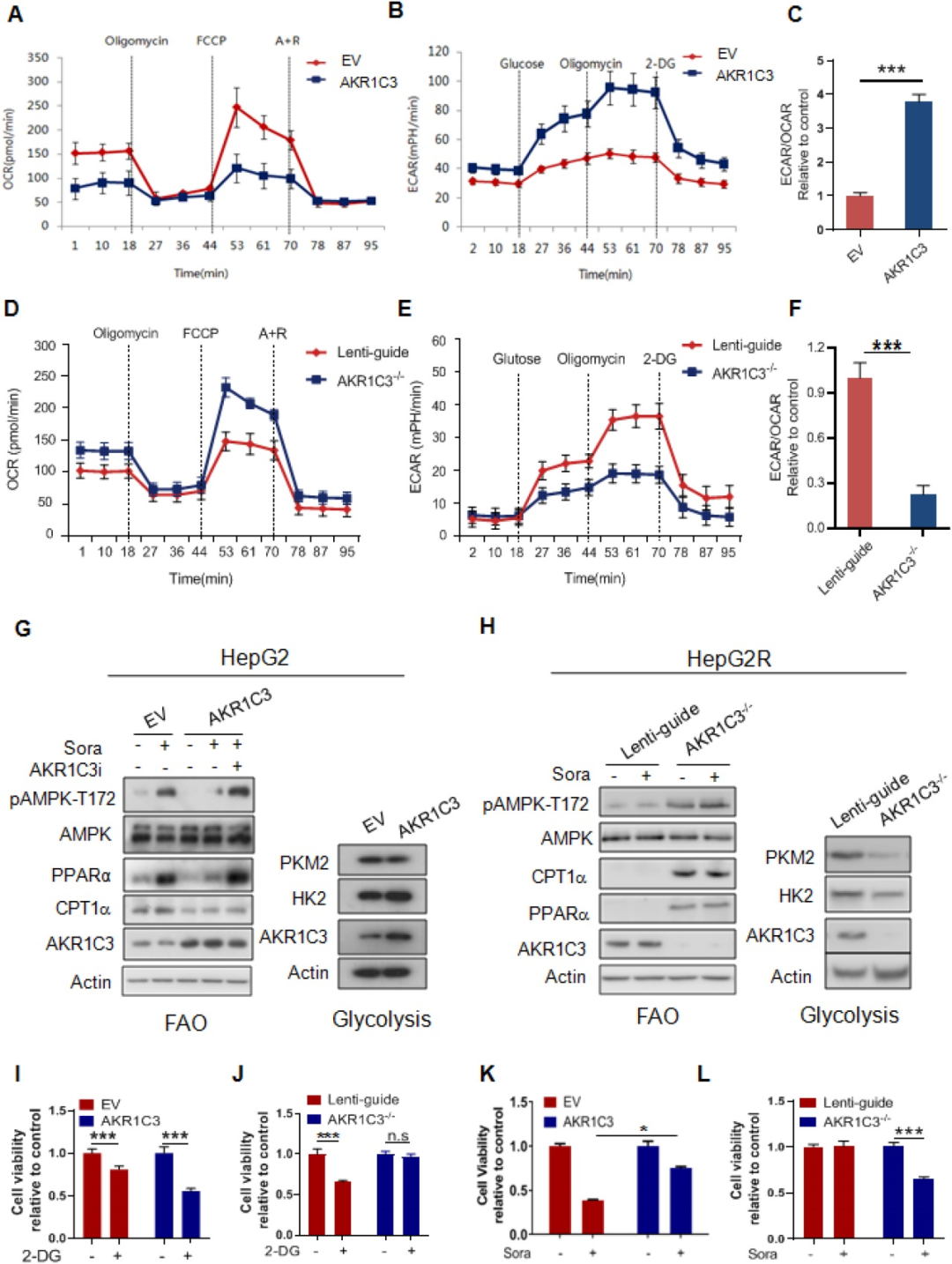
为了检测AKR1C3是否会影响能量代谢,研究者对原始癌细胞中过表达AKR1C3或在抗性癌细胞中敲低AKR1C3。过表达AKR1C3后,原始癌细胞的耗氧率(OCR)下降,细胞外酸化率(ECAR)上升,ECAR/OCR比值上调3.7倍。在抗性癌细胞中敲低AKR1C3后,耗氧率(OCR)上升,细胞外酸化率(ECAR)下降,,ECAR/OCR比值下降2倍。此外,过表达AKR1C3降低了AMPK-T172磷酸化、PPARα和CPT1A的水平,但增加了HK2的蛋白水平。而AKR1C3的抑制恢复了索拉非尼处理的癌细胞中上述蛋白的水平。此外,与对照细胞相比,高表达AKR1C3的HepG2细胞对葡萄糖表现出更大的生长依赖性。相反,与对照组相比,AKR1C3-/- HepG2R细胞对葡萄糖的敏感性较低。最后,在索拉非尼处理条件下,AKR1C3过表达明显提高了HepG2细胞的存活率,而敲除AKR1C3使HepG2R细胞对索拉非尼敏感。这些结果表明,AKR1C3使代谢从脂肪酸氧化转向糖酵解,以促进HCC细胞对索拉非尼的抗性。
7. AKR1C3维持索拉非尼处理条件下肝细胞癌细胞的生长
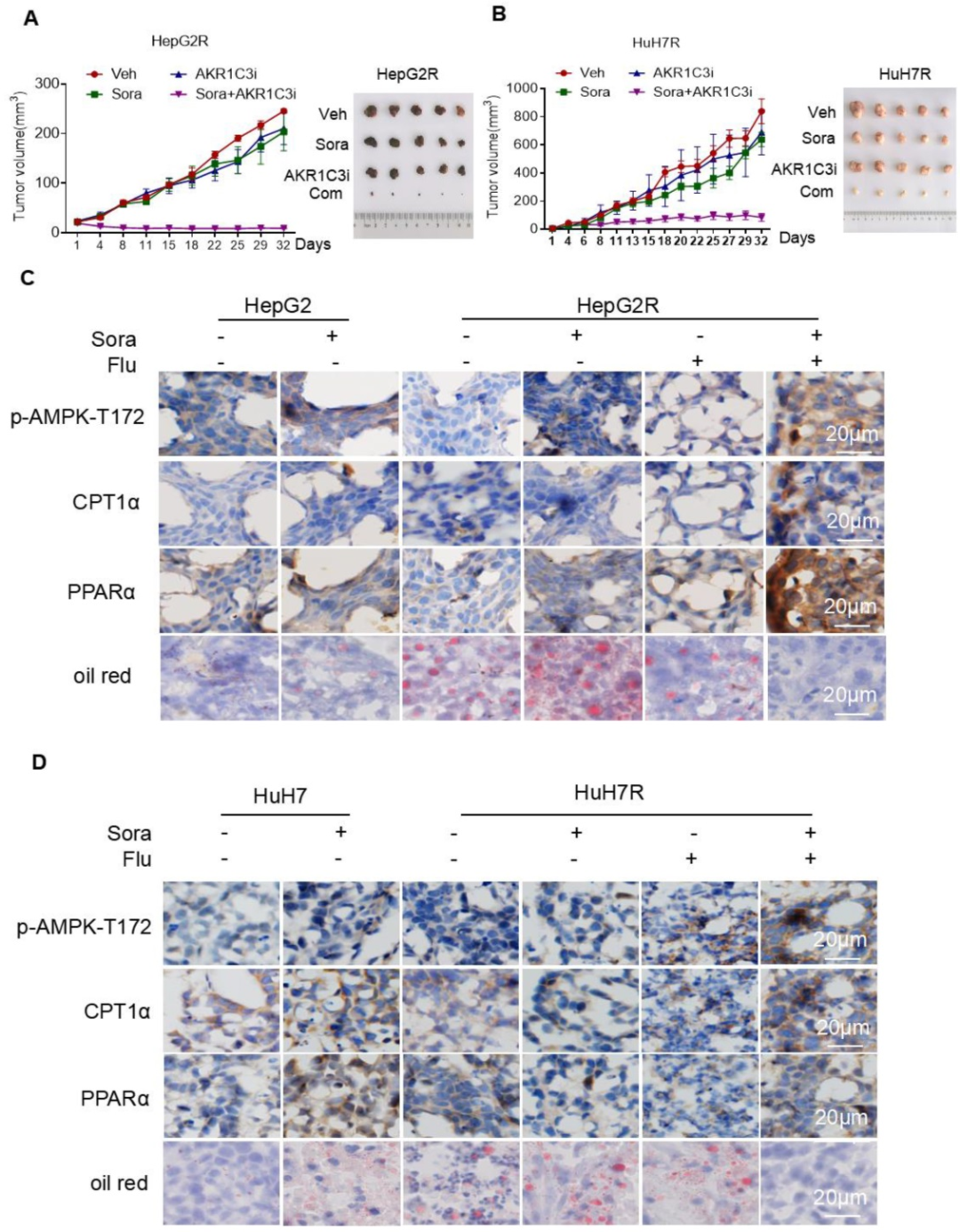
接下来,研究者探究了索拉非尼和FLU (氟芬那酸,AKR1C3抑制剂)联合治疗对肝细胞癌细胞的影响。结果表明,联合治疗强烈地抑制了抗性癌细胞HepG2R和HuH7R异种移植瘤的生长。免疫组化显示CPT1A和PPARα的表达明显升高,提示细胞存在脂滴分解。油红染色实验证明,联合治疗降低了肝细胞癌细胞异种移植肿瘤中的脂滴积累。进一步,研究者观察了AKR1C3-/-HepG2R移植瘤小鼠的肿瘤生长情况。结果表明,AKR1C3缺失与索拉非尼协同作用,通过诱导脂肪吞噬来抑制肿瘤生长。以上基于肝细胞癌细胞异种移植瘤模型的研究表明,抑制AKR1C3会诱导脂滴分解和线粒体脂质毒性,从而使耐药的肝细胞癌细胞对索拉非尼敏感。
研究总结
本研究发现,长期的索拉非尼治疗会损害脂肪酸氧化(FAO),导致肝细胞癌(HCC)细胞中脂滴(LD)的积累。对索拉非尼抗性和原始癌细胞的脂质组学和蛋白质组学联合分析发现,醛酮还原酶AKR1C3是肝细胞癌中脂滴积累的重要调控基因。AKR1C3缺失完全消除脂滴含量,使游离脂肪酸流向磷脂、鞘脂和线粒体。此外,研究者发现AKR1C3依赖的脂滴积累是缓解索拉非尼诱导的线粒体脂肪毒性和功能障碍的必要条件。药物抑制AKR1C3的活性会立即诱导自噬依赖的脂滴分解,导致线粒体裂变和索拉非尼抗性肝细胞癌细胞凋亡。改变AKR1C3的表达足以驱动脂肪酸氧化和糖酵解之间的代谢转换。AKR1C3可作为肝细胞癌治疗的一个潜在靶标。
吉凯基因凭借多年在靶标筛选及验证服务领域的技术积累,建立的标准化 、工程化 、系统化的GRP平台,为中国研究型医生提供科研服务,加快科研成果转化。其中,多组学平台包含蛋白质组学平台和高通量测序平台:
·蛋白质组学平台拥有多台timsTOF Pro、Exploris 480高精度质谱仪,专业的Spectronaut Plusar、Mascot等分析软件,提供专业的4D、DIA、TMT、PRM、磷酸化修饰组、olink蛋白质组等检测服务,强大的机器学习算法、IPA分析、蛋白基因组分析服务,系统的生物标志物、分子分型、药物靶点、基因功能研究等解决方案,真正让广大研究型医生的科研工作更省心、更省力、更高效;
·高通量测序平台分为常规测序服务和单细胞测序服务:单细胞测序拥有10x和BD两个平台,提供单细胞RNA-seq、单细胞核测序、单细胞混样RNA-seq、单细胞TCR/BCR、单细胞(RNA+ATAC)、空间转录组测序等服务;常规测序服务提供meRIP-seq(m6A/m1A/m7G/m5C 等RNA甲基化修饰测序)、acRIP-seq(ac4C RNA乙酰化修饰测序)、ATAC-seq、Ribo-seq(翻译组测序) 、mRNA/miRNA/LncRNA/circRNA-seq、全转录组测序(两文库/三文库)、外泌体miRNA/LncRNA-seq、WGS/WES、WGBS、RRBS、BSAS等服务。
